Årets Medeonstipendiat heter Lena Eliasson, forskare vid Lunds universitets Diabetescenter i Malmö. Läs en förkortad version av det föredrag hon höll på Medeondagen.
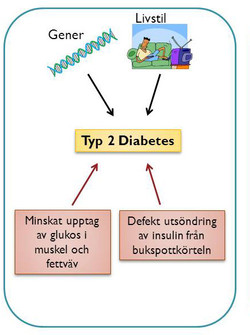
Typ 2 diabetes beror både på genetiska faktorer och livsstilsfaktorer. Dessa leder till:
1) upptaget av glukos i muskel och fettväv, där det har sin verkan, försämras – vilket benämns insulinresistens
2) utsöndringen av insulin från bukspottkörteln är defekt. Den här presentationen kommer framförallt behandla kopplingen mellan insulinsekretion och uppkomsten av typ2 diabetes.
Försämrad insulinutsöndring
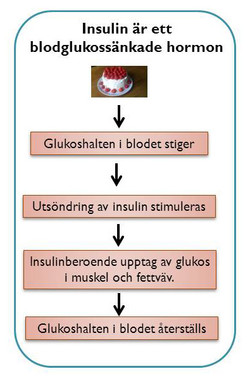
Insulin är det hormon i kroppen som medverkar till att sänka blodsockernivåerna när vi ätit. Utsöndringen stimuleras av att glukoshalten i blodet stiger och väl i blodet forslas insulin till målvävnaderna muskel och fettväv, där det behövs för att glukos ska kunna tas upp av dessa celler för att till exempel medverka till att ge energi till våra muskler. Insulin fungerar som en nyckel så att glukos kan komma in i cellen.
Den senaste tidens genetiska studier har visat på att ett flertal av de genvarianter som ökar risken för att få typ 2 diabetes är kopplade till en försämrad utsöndring av insulin.
Uttröttade celler
Vidare finns det också flera studier som tyder på att utsöndringen av insulin försämras på grund av att cellerna blir utslitna. Då vi äter med täta intervall och mat/godis/kakor med högt sockerinnehåll, leder detta till slut till att systemet slits ut och de insulinproducerande betacellerna orkar inte med att kunna kompensera för förhöjda blodsockernivåer.
I de flesta fall är det med stor sannolikhet en kombination av båda två.
En miljon öar
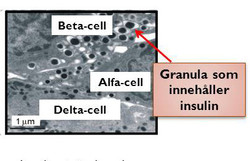
Betacellerna, som finns i små cellklumpar, är utspridda i bukspottkörteln och kallas för Langerhanska öar. En bukspottkörtel innehåller cirka en miljon öar och varje ö cirka 1 500 betaceller.
I de langerhanska öarna finns också celler som bildar glukagon. Detta hormon frigörs då koncentrationen av blodglukos är låg och har motsatt effekt till insulin; det vill säga det medverkar till att höja glukosmängden i blodet vid fasta eller då vi är fysiskt aktiva genom att bland annat frigöra glukos från lagren i levern.
Även utsöndringen av glukagon är störd vid diabetes och det är vanligt att patienter med typ 2 diabetes har en förhöjd utsöndring av glukagon vilket förvärrar situationen.
En tredjedels miljondels meter
Insulin finns lagrat i cellen i små blåsor eller kapslar som kallas granula. Varje cell innehåller ca 10 000 granula och varje granula är 300 nanometer i diameter (1/3 miljondels meter). Av dessa 10 000 granula finns ungefär tio procent nära cellmembranet, redo att släppa ut insulin till blodet direkt när de får en signal att göra det. Och hur sker det?
Likheter med nervcellerna
Insulin tar sig ut i blodet genom att dessa granula smälter samman med cellmembranet i en process som kallas exocytos. Denna process startas av att mängden kalcium ökar inne i cellen. Att kalcium kommer in beror på en elektrisk signal som startas av att glukos tas upp i betacellen. Betacellen är en elektrisk cell precis som nervcellerna och utsöndringen av insulin har många likheter med utsöndringen av neurotransmittor i hjärnan.
Vi undersöker detta med en teknik som kallas patch-clamp, den gör det möjligt att mäta strömmar i enskilda celler, vilka är en miljarddels gånger lägre än strömmen i lamporna hemma.
Som när strömmen går
När det elektriska regleringssystemet inte fungerar eller när komponenter som är viktiga i den exocytosprocess inte fungerar tillfredställande, är det som när det strömmen går; spisen fungerar inte, lampan lyser inte.
När lampan inte lyser hemma eller spisen inte fungerar börjar vi leta efter var felet är. Det kan vara en propp, det kan var spisen, det kan vara en platta. På så sätt hittar vi orsaken till varför inte spisen fungerar.
På liknande sätt kartlägger vi den process som leder till utsöndring av insulin för att få en förståelse för hur processen går till och också hitta var i denna process det går snett vid uppkomsten av diabetes.
Små korta molekyler
För att justera utsöndringen av insulin kan kroppen reglera de proteiner som medverkar i processen. Uttrycket (dvs. produktionen) av protein kan regleras på flera sätt varav ett sker via cellens egna reglersystemmolekyler – microRNA. Dessa är små korta molekyler som finns i arvsmassan och de reglerar uttryck av protein både kortsiktigt och långsiktigt.
Vi har visat att ett antal av dessa microRNA är reglerade av glukos och att de har ett högre uttryck i en diabetisk djurmodell*. Vidare har vi visat att en djurmodell, som inte kan göra fullständiga microRNA i betacellen, får diabetes. Båda dessa studier visar på en central roll för microRNA .
MicroRNA kan också användas som biomarkörer och vi har tecken på att ett visst microRNA ökar i blodet hos råttor som utvecklar diabetes. Finns det i blodet kan man mäta det på ett enkelt sätt och ställa tidigare diagnoser.
Betacellen tar upp fett från maten
Hur påverkas då betacellerna och utsöndringen av insulin av den mat vi äter, av för mycket fett och kolhydrater?
Vi har indikationer att betacellerna tar upp fett och att antalet fettdroppar inne i betacellerna ökar med förhöjt BMI (övervikt). Om detta är en skyddande effekt eller inte vet vi inte. Det kan ju vara så att formationen av fettdroppar är ett sätt att skydda cellen från de fria fettsyrorna.
Det är visat att insulinsekretionen och exocytosen försämras i beta-celler efter förvaring i höga halter palmolja.
Kortsiktigt ökar både fett som palmolja och glukos insulinsekretionen, men kroniskt höga halter har negativa effekter på utsöndringen av insulin och specifikt också på exocytosprocessen.
Hitta lämpliga läkemedel
Varför är det då viktigt att studera insulinsekretion på cellulär nivå? Vår förhoppning är att genom att ta reda på hur processen går till så kan vi också hitta lämpliga läkemedel som kan påverka processen att öka utsöndringen av insulin vid diabetes.
Då man utmanar betacellerna i kroppen att utsöndra insulin genom att tillföra en viss mängd glukos i ett svep utsöndras insulin i två faser, en första snabb fas och en andra långsammare.
Hos en diabetiker är första fasen borta eller mycket låg. Cellulärt har vi genom vår och andras forskning kunnat koppla detta till den process där insulingranula gör sig klara för att sammansmälta med membranet som omger cellen.
Vi har förhoppningar om att finna läkemedel som kan påverka denna process.
Tarmhormonernas positiva effekter
Ett sådant finns redan ute i handeln sedan ett antal år tillbaka. GLP1-analoger liknar det hormon som kallas GLP-1 och utsöndras från celler i tarmen när vi äter. Vi har bland annat kunnat visa på att GLP-1 stimulerar processen som föregår exocytos, vilket kan läggas till andra positiva effekter av GLP-1.
Likaså har GIP, ett annat hormon som utsöndras av celler i tarmen, positiva effekter på exocytosprocessen.
Vi har också visat att GIP, genom att binda till GIP-receptorn (och öka intracellulärt cAMP) bidrar till minskad celldöd. Patienter med en specifik variant av den receptor som GIP binder till på beta-cellens yta har försämrad insulinsekretion.
Olika sjukdomsvarianter
Slutligen vill jag också nämna en av våra senaste studier som tydligt visar på att typ 2 diabetes inte är en sjukdom utan finns i flera varianter. Detta innebär säkerligen också att vi i framtiden går mot en mer individualiserad behandling.
I vår studie har vi genom att studera exocytosprocessen funnit att i betaceller från människa är det bara vissa genetiska riskvarianter som leder till en försämrad exocytosprocess; andra genetiska riskvarianter har troligen andra cellulära effekter.
Slutsatser
Diabetes beror delvis på försämrad utsöndring av insulin.
Felaktig kosthållning kan leda till utslitning av betacellerna så att de inte längre förmår att utsöndra tillräckligt med insulin för att hålla blodsockret på normal nivå.
Genetiska varianter, som ökar risken för diabetes och är associerade med försämrad insulinsekretion, kan ha olika cellulära effekter.
Text, foto och illustrationer: LENA ELIASSON
* med diabetisk djurmodell menas försöksdjur som har diabetes
Artikeln är tidigare publicerad på Diabetesportalen, 25 maj 2012